López-Valero I, Dávila D, González-Martínez J, Salvador-Tormo N, Lorente M, Saiz-Ladera C, Torres S, Gabicagogeascoa E, Hernández-Tiedra S, García-Taboada E, Mendiburu-Eliçabe M, Rodríguez-Fornés F, Sánchez-Domínguez R, Segovia JC, Sánchez-Gómez P, Matheu A, Sepúlveda JM, Velasco G.
Midkine signaling maintains the self-renewal and tumorigenic capacity of glioma initiating cells.
Theranostics. 2020 Apr 6;10(11):5120-5136.
DOI: 10.7150/thno.41450.
RESUMEN
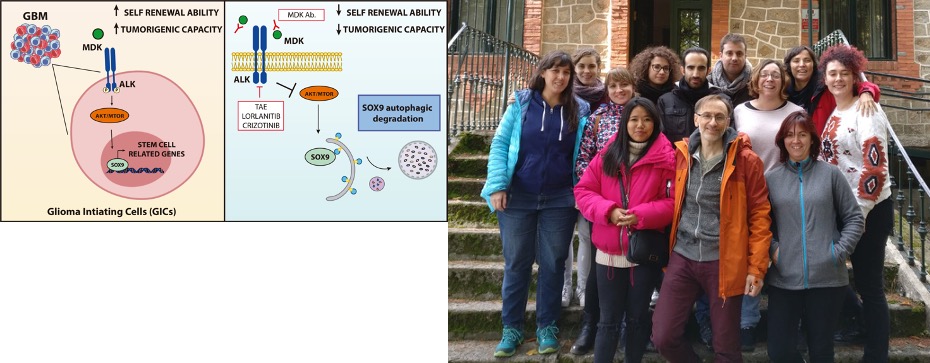
Se trata de un artículo en el que identificamos el papel de la proteína Midquina (MDK) y su receptor (ALK) en "Glioma initiating cells" (GICs, células madre derivadas de un tipo de tumor cerebral muy agresivo denominado Glioblastoma, GBM). Se sabe que las GICs son particularmente resistentes a la mayor parte de tratamientos antitumorales permanecen en los tumores tras su resección siendo por tanto responsables de las recaídas que ocurren casi en el 100% de los pacientes con este enfermedad. En el estudio encontramos que los niveles de MDK están elevados en las células GICs y que esta proteína podría ser un biomarcador de mal pronóstico en este tipo de tumores. También encontramos que la MDK puede ser una diana terapéutica para el tratamiento del GBM. Así nuestros datos muestran que la inhibición de la señal que produce la MDK bloquea la replicación de las GICs. Más aún, cuando combinamos la inhibición de la MDK o de su receptor ALK con temozolomida (TMZ, el fármaco que se utiliza habitualmente para el tratamiento del GBM) o con THC o THC y CBD (dos cannabinoides con los que trabajamos habitualmente en el laboratorio) podemos eliminar completamente esta población de células GICs. Igualmente experimentos desarrollados en modelos animales de GBM confirman que el bloqueo de la señal a través del eje MDK/ALK produce un potente efecto antitumoral per se y potencia la acción de la Temozolomida. En el trabajo también identificamos el mecanismo por el que la MDK regula la capacidad de autorrenovarse de las GICs (esta es una característica típica de las células madre tumorales que les permite permanecer en los tumores y dar lugar a las recaídas). Dicho efecto se debe a la capacidad de la MDK y su receptor para controlar la activación de la autofagia y la degradación de el factor de transcripción SOX9. Finalmente mencionar que el trabajo ha contribuido a sentar las bases de un ensayo clínico desarrollado por el Grupo Español de Investigación en Neuroncología (GEINO) en el que se ha analizado el efecto del fármaco crizotinib (un inhibidor de ALK) en combinación con temozolomida y radioterapia en pacientes con Glioblastoma de reciente diagnóstico. Los resultados de este ensayo clínico serán publicados en los próximos meses. El estudio, cuyo desarrollo ha sido la base de la tesis de Israel López Valero - el primer autor del artículo - se ha desarrollado con la participación de varios investigadores de nuestro grupo de investigación del Departamento de Bioquímica y Biología Molecular de la Facultad de Biología de la UCM y el Instituto de Investigaciones sanitarias San Carlos incluyendo a David Dávila (co-primer autor del trabajo), José González, Nélida Salvador, Mar Lorente, Cristina Saiz, Sofía Torres, Estibaliz Gabicagogeascoa, Sonia Hernández, Elena García, Marina Mendiburu-Eliçabe. Además para el desarrollo del trabajo hemos contado con la colaboración del Neuroncólogo Juan Sepúlveda (del Hospital 12 de Octubre) así como de los investigadores Pilar Sánchez (del Instituto de salud carlos III de Madrid), Ander Matheu (del Instituto Biodonostia de San Sebastián) así como de Fátima Rodríguez, Rebeca Sánchez y José Carlos Segovia (del Centro de Investigaciones Energéticas, Medioambientales y Tecnológicas de Madrid).