Palacios-Ortega J, García-Linares S, Rivera-de-Torre E, Heras-Márquez D, Gavilanes JG, Slotte JP, Martínez-Del-Pozo Á.
Structural foundations of sticholysin functionality.
Biochim Biophys Acta Proteins Proteom. 2021 Oct;1869(10):140696
DOI: 10.1016/j.bbapap.2021.140696
RESUMEN
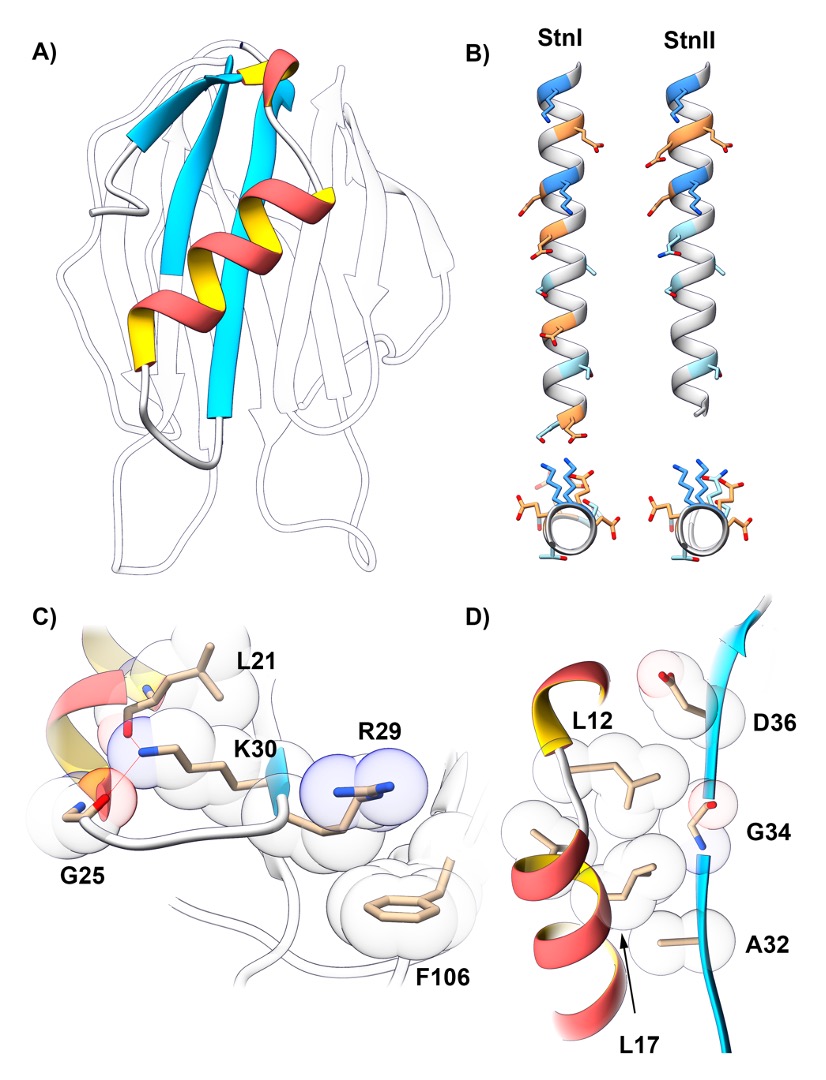
Las actinoporinas, producidas por anémonas marinas, constituyen una familia de proteínas tóxicas formadoras de poros. Estas toxinas ejercen su actividad mediante el reconocimiento específico de esfingomielina en las membranas. La estructura hidrosoluble de estas proteínas consiste en un sándwich β flanqueado por dos hélices α. Cuando se produce la unión a la membrana, estas proteínas perforan la bicapa lipídica mediante la inserción de la hélice α localizada en el extremo N-terminal de su secuencia. Este proceso, que conduce a la formación de poros selectivos de cationes, provoca que las células afectadas acaben muriendo por el choque osmótico al que se ven sometidas. En esta revisión, se examina como las características estructurales de estar toxinas intervienen en su funcionalidad, haciéndose hincapié en los residuos que, dada su relevancia, presentan un mayor grado de conservación. Siguiendo los últimos descubrimientos del campo, también se analizan los requisitos moleculares de la membrana, el efecto de su composición lipídica y el propio proceso de formación de los poros.